上海云序生物科技有限公司
Shanghai Cloud-seq Biotech Co., Ltd.
地址:上海市松江区莘砖公路 518 号 20 号楼 3 楼
电话:021-64878766
传真:021-64878766
网址:www.cloud-seq.com.cn
邮箱:market@cloud-seq.com.cn
肝脏病学权威杂志Hepatology (IF=14.97)在线发表了一项最新研究成果:RNA甲基化在NAFLD发生发展中起着重要的作用。该文当中m6A-seq和RNA-seq由云序生物提供技术服务。据悉,复旦大学附属中山医院内分泌科团队长期致力于NAFLD的发病机制研究,在近期工作中系统性阐明了多个与肝脏代谢相关的分子机制(PNAS 2019、Diabetes 2018、 Diabetes 2017、Cell Metabolism 2016、JCI 2014、Gut 2014)。本期我们解析该课题组2019年10月应用云序生物的RNA-seq技术服务,发表在PNAS杂志(IF 9.58)上关于内质网应激对2型糖尿病影响的文章。
2型糖尿病的发病机制主要是胰岛素抵抗(IR)和胰岛β细胞功能受损,已有研究提出内质网应激(ERS)是导致糖尿病、IR和肥胖发生的主要途径。内质网应激是指由于某种原因使细胞内质网生理功能发生紊乱的一种亚细胞病理状态。多种因素可以打破内质网的稳态,导致蛋白质折叠障碍或错误折叠,进而触发内质网应激。适度的内质网应激会导致适应性的细胞保护作用,过高和持久的内质网应激则会激活特有的凋亡通路导致细胞凋亡。内质网应激通过影响胰岛细胞的功能,促使胰岛β细胞凋亡及参与胰岛素抵抗介导2型糖尿病的发生和发展。该研究显示了内质网应激诱导的葡萄糖稳态破坏的机制,并提出USP14作为针对T2DM的潜在治疗靶标。


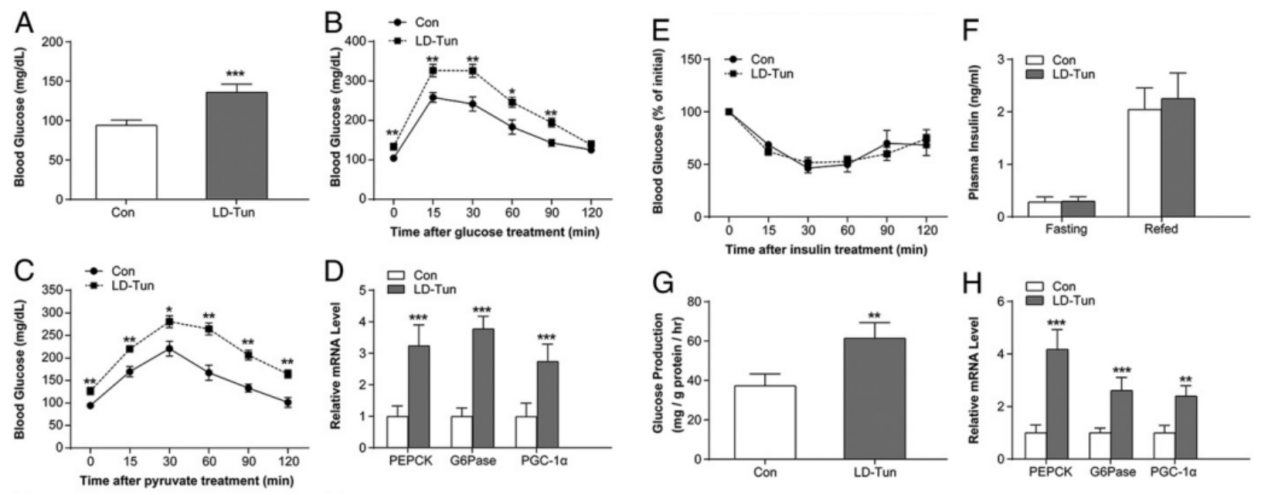
图1. 持续的内质网应激会诱发高血糖症和肝糖异生
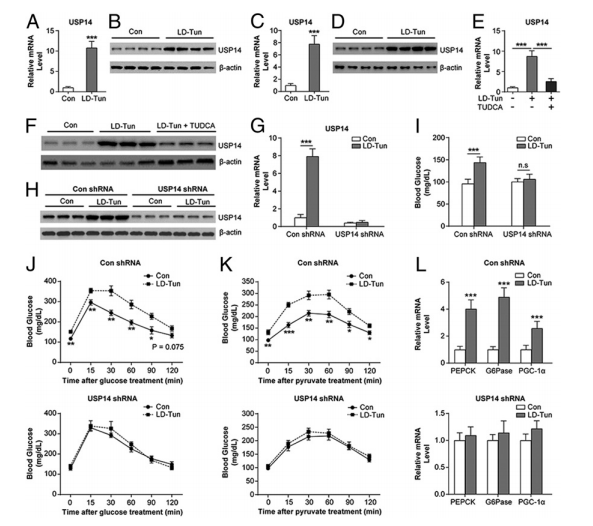
图2. 持续内质网应激的糖原异生作用需要USP14
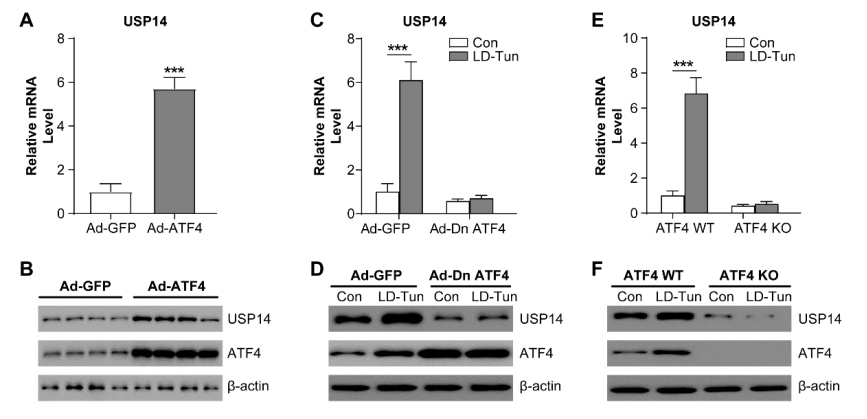
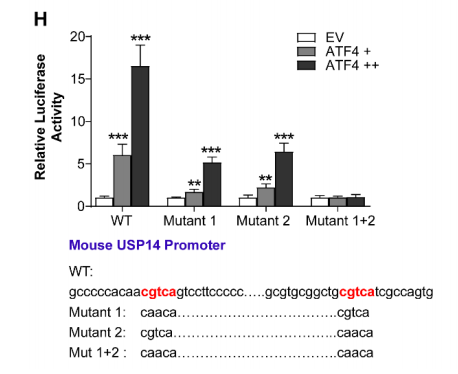
图3. 持续的内质网应激通过ATF4上调USP14
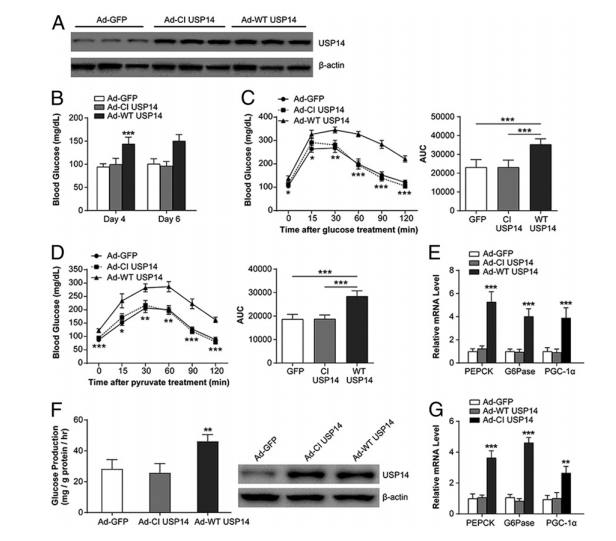
图4. 肝USP14的过表达引起高血糖症并促进糖异生
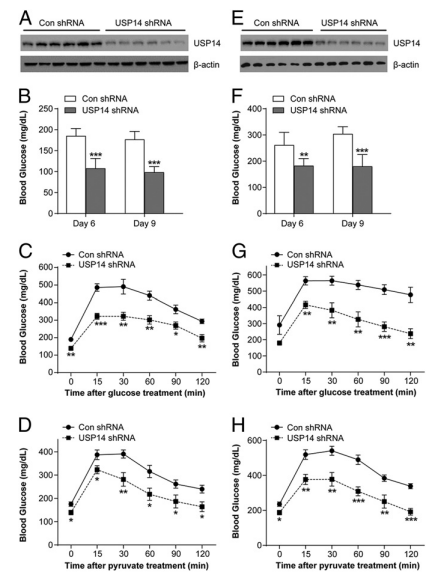
图5. 抑制肝脏USP14可改善肥胖小鼠的葡萄糖代谢
(6)USP14通过提高胰高血糖素作用来增加肝糖异生
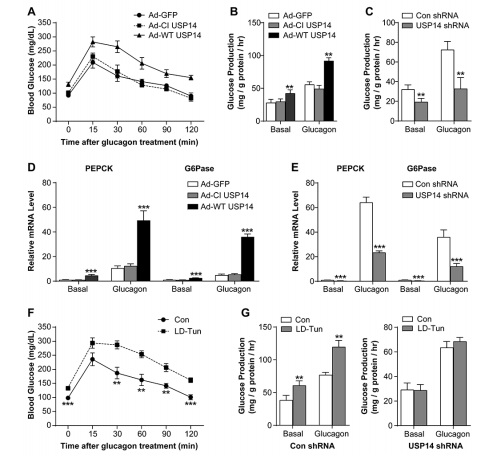
图6. USP14通过提高胰高血糖素作用来增加肝糖异生
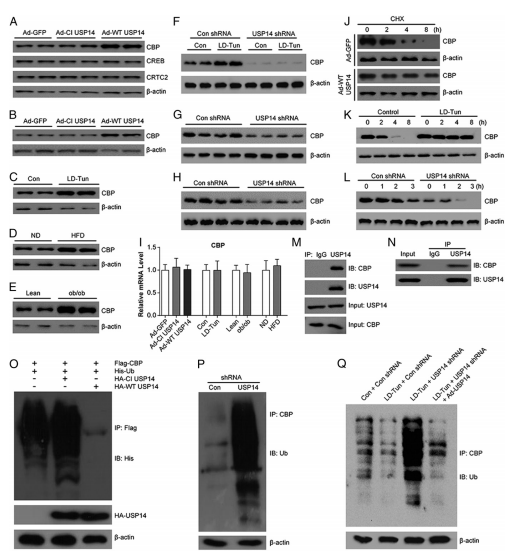
图7. USP14提高CBP稳定性

地 址: 上海市松江区莘砖公路518号24号楼4楼 联系人: 戴小姐 电 话: 021-64878766 传 真: 021-64878766 Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
杨宝峰院士团队RNA修饰又一成果 | 云序ac4C acRIP-seq助力揭示心脏I/R损伤的作用机制
(2024-12-03T00:00 浏览数:2712)
杨宝峰院士团队最新成果 | 云序助力揭示RNA修饰m7G调控心肌肥厚的机制研究
(2024-11-13T00:00 浏览数:4575)
Nature子刊| 重磅综述!一文总结「m6A修饰非编码RNAs」在各类肿瘤中的调控机制及作用
(暂无发布时间 浏览数:4298)
研究速览-eccDNA 2023年最新进展大放送!
(暂无发布时间 浏览数:3950)
云序生物MeRIP-qPCR技术干货
(暂无发布时间 浏览数:3977)
技术干货| “eccDNA碱基序列的获取及引物设计”方法教程
(暂无发布时间 浏览数:4281)
云序客户m6A高分文章|揭示组蛋白乙酰化与m6A修饰在眼部黑色素瘤发生中的共同作用机制
(暂无发布时间 浏览数:3025)
Nat Biotechnol IF=47 | BID-seq:一种基于单碱基分辨率的假尿嘧啶(Ψ)修饰定量测序检测方法
(暂无发布时间 浏览数:2681)
北大伊成器团队Nature Reviews重磅发文:非m6A热门修饰调控与功能一文速览!
(暂无发布时间 浏览数:3802)
用户文章m6A专题|IF=9.8|m6A去甲基化酶ALKBH5缺乏会加重钴致神经退行性损伤
(暂无发布时间 浏览数:2596)
上海云序生物科技有限公司
商家主页
相关咨询
