脓毒症是一种由感染引起的全身性炎症反应综合征,常导致多器官功能障碍,其中肝脏损伤是独立的风险因素,与高死亡率相关,目前针对脓毒症相关肝损伤的病理机制和治疗策略尚未完全明确。时间限制性进食(TRF)这一饮食干预方式因其在代谢调控方面的显著效益而备受关注,将每日进食时间控制在特定窗口期的饮食模式,已被证实能够改善胰岛素敏感性、减轻慢性炎症等。TRF是否能够通过特定机制对脓毒症肝损伤产生保护作用这方面研究尚无人涉足。
2025年4月,南方医科大学南方医院刘克玄教授团队在Gut Microbes上在线发表了题为“Time-restricted feeding protects against septic liver injury by reshaping gut microbiota and metabolite 3-hydroxybutyrate”的研究文章,通过代谢组学、微生物组学、转录组学等多组学手段,揭示了限时饮食(TRF)可通过重塑肠道菌群,增加3-羟基丁''酸(3-HB)水平,激活PI3K/AKT/mTOR/LPIN1通路抑制肝细胞铁死亡,减轻脓毒症肝损伤,为临床该疾病的防治提供新方向。(麦特绘谱提供Q200宏代谢技术检测服务)

研究设计
• 动物模型:盲肠结扎穿刺(CLP)和脂多糖(LPS)注射诱导脓毒症小鼠模型
• 实验分组:TRF(6小时进食/18小时禁食)vs正常饮食(ND),结合抗生素(ABX)处理、粪菌移植(FMT)、无菌(GF)小鼠及基因敲除(Hmgcs2/Lpin1)小鼠
• 临床样本:57例脓毒症患者(17例肝损伤 vs 40例非肝损伤),检测粪便L. murinus丰度和血清3-HB水平
• 实验方法:Q200宏代谢组学、16S、转录组学、分子互作、功能实验等
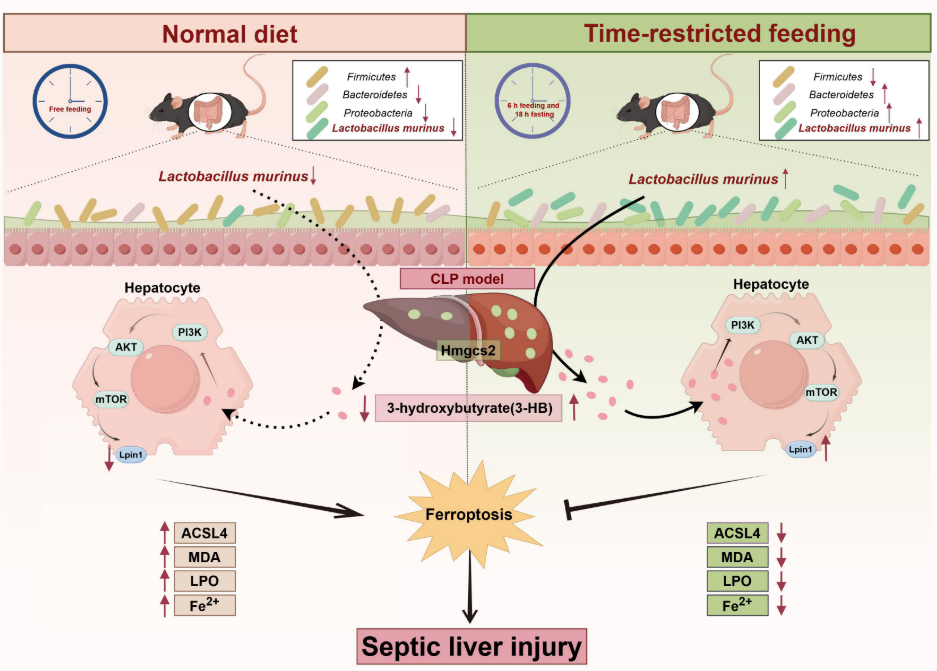
研究思路
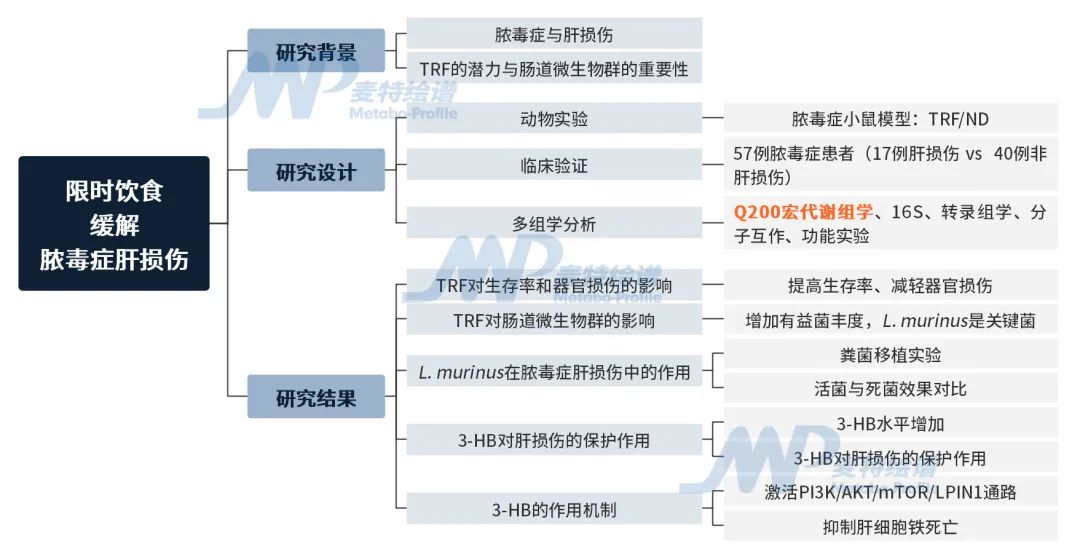
研究结果
1.TRF减轻脓毒症损伤并重塑肠道菌群
TRF显著提高了CLP小鼠的存活率,降低了血清内毒素水平,并减轻了肝脏、肺和肾脏的损伤。16S rRNA基因测序显示,TRF显著改变了肠道微生物群的组成和多样性,特别是增加了Lactobacillus murinus(L. murinus)的丰度。
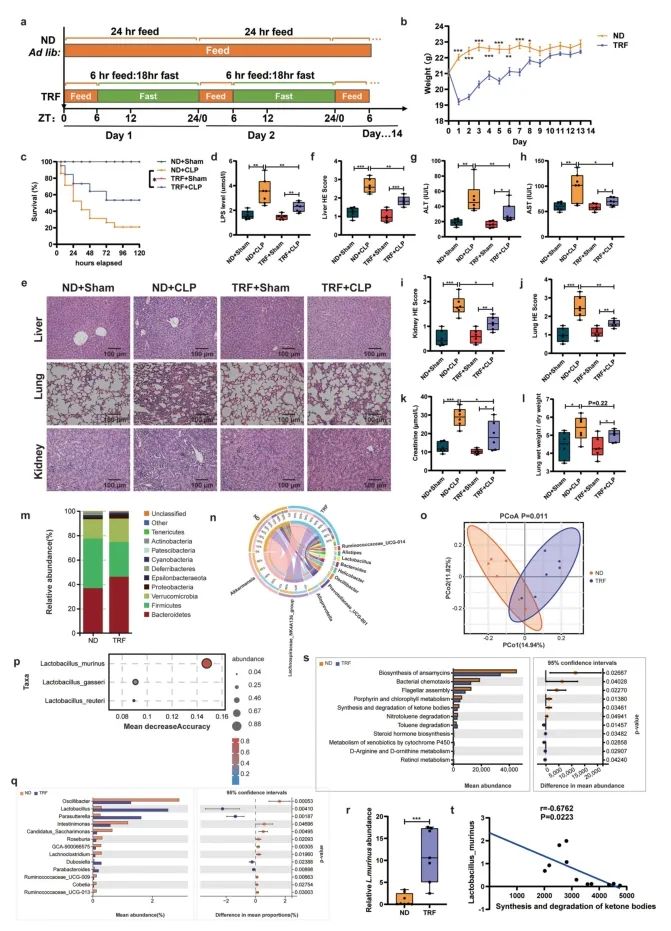
图1. 限时喂养减轻脓毒症损伤并改变肠道微生物群组成和多样性
2.L. murinus对脓毒症肝损伤的保护作用
通过粪菌移植(FMT)实验,发现TRF处理的小鼠粪便能够改善脓毒症小鼠的存活率和肝损伤。在无菌鼠(GF)实验中,L. murinus的灌胃显著降低了血清LPS水平和肝损伤。与灭活的L. murinus相比,活的L. murinus预处理能够显著降低血清LPS、ALT和AST水平,并减轻肝损伤,表明L. murinus通过活性代谢物发挥作用。通过Q200宏代谢组学分析(麦特绘谱提供)显示L. murinus处理显著提升脓毒症小鼠盲肠和血清中的3-羟基丁''酸(3-HB)水平,且3-HB与肝损伤标志物呈负相关。除此之外,3-HB合成必需酶Hmgcs 2(3-羟基-3-甲基戊二酰辅酶A合成酶2)的表达趋势与3-HB的表达趋势一致。
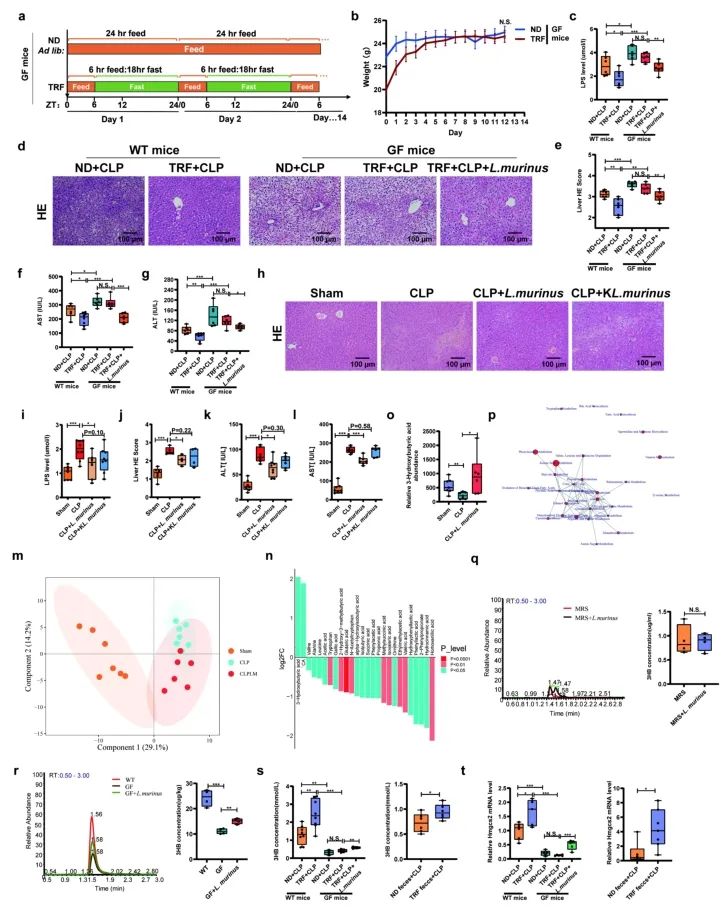
图2. L. murinus减轻肝损伤
3.临床相关性验证
脓毒症肝损伤患者血清3-HB水平和粪便L. murinus丰度显著低于非肝损伤组,3-HB与ALT/AST负相关,ROC曲线显示其预测肝损伤的AUC=0.8429。
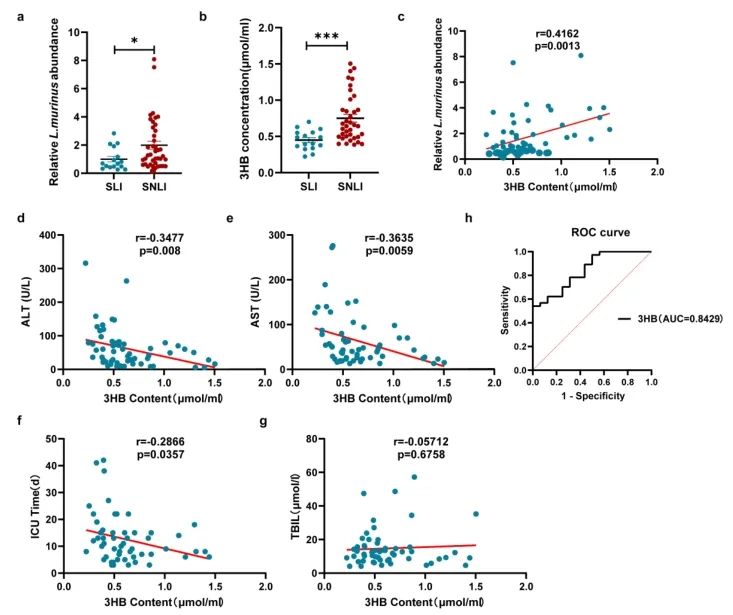
图3. 脓毒性肝损伤患者血清3-HB水平与肝损伤标志物的相关性分析
4.L. murinus通过宿主Hmgcs2促进3-HB生成
进一步通过Hmgcs2基因敲除小鼠模型来验证,发现与假手术小鼠相比,CLP小鼠肝脏中HMGCS2表达降低,活的L. murinus预处理可上调HMGCS2表达,增加血清3-HB水平,灭活的L. murinus无此效果。进一步通过AAV病毒介导的Hmgcs2基因敲除实验发现,Hmgcs2敲除小鼠中L. murinus无法恢复3-HB水平,也无法减轻脓毒症肝损伤,表明Hmgcs2在L. murinus的保护作用中不可或缺。
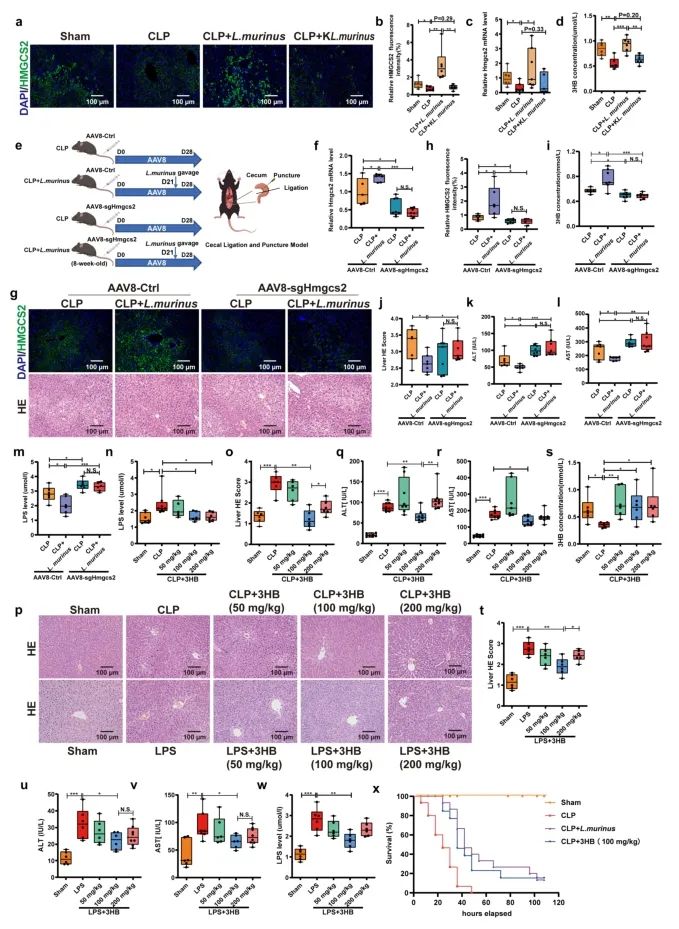
图4. L. murinus通过Hmgcs2酶促进3-HB合成以减轻脓毒性肝损伤
5. 3-HB通过PI3K/AKT/mTOR/LPIN1抑制铁死亡
转录组测序结果显示,3-HB处理显著上调Lpin1基因表达。KEGG通路富集分析表明PI3K/AKT通路在3-HB处理组显著激活。Western blot证实3-HB促进AKT/mTOR磷酸化及PI3K、LPIN1蛋白表达,分子对接和SPR实验证明3-HB直接结合PI3K蛋白。使用PI3K/AKT/mTOR抑制剂NVP-BEZ235可逆转3-HB的肝保护作用。在Lpin1敲除小鼠中,3-HB未能改善CLP诱导的肝损伤和炎症因子(IL-1β、IL-6、TNF-α)升高。这些结果表明,3-HB通过直接靶向PI3K,激活PI3K/AKT/mTOR/LPIN1信号通路,从而减轻脓毒症肝损伤。此外,GSEA-KEGG分析显示铁死亡通路在脓毒症模型(CLP组)显著激活,3-HB处理可下调关键铁死亡标志物ACSL4的表达,并降低肝脏MDA、LPO和Fe²⁺水平。LPIN1作为该通路下游关键分子,其敲除小鼠中3-HB的抗铁死亡作用完全消失。此外,铁死亡抑制剂Fer可减轻肝损伤,而NVP-BEZ235的恶化作用可被Fer逆转。这些结果证实3-HB通过PI3K/AKT/mTOR/LPIN1信号轴抑制铁死亡,从而发挥肝保护作用。
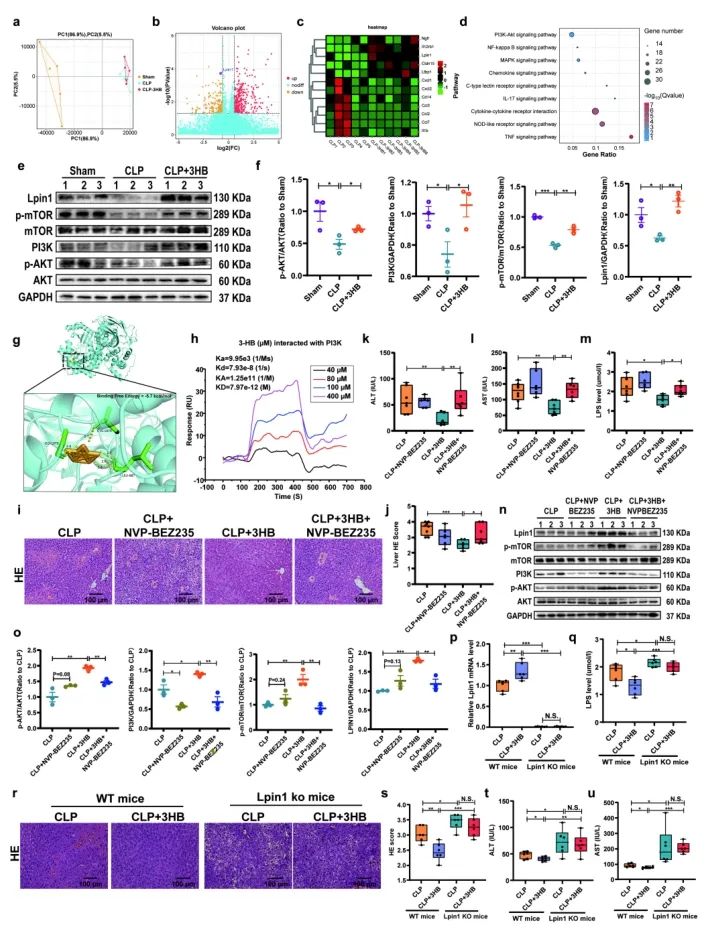
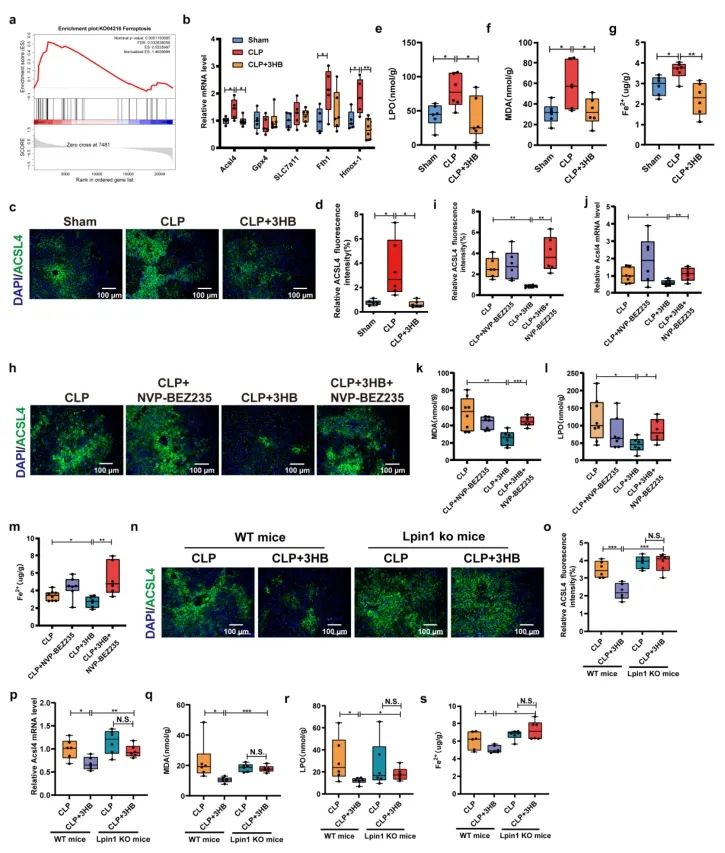
图5. 3-HB通过PI3K/AKT/mTOR/LPIN1抑制铁死亡
6.体外验证
AML12细胞中,3-HB处理显著提高了细胞活力,降低乳酸脱氢酶(LDH)含量,同时也降低了LPS诱导的丙二醛(MDA)、脂质过氧化(LPO)和Fe²⁺水平,增加了总谷胱甘肽(TGSH)含量,使用PI3K/AKT/mTOR通路抑制剂也进一步证实了3-HB通过激活PI3K/AKT/mTOR/LPIN1减少LPS诱导的铁死亡,从而减轻细胞损伤。
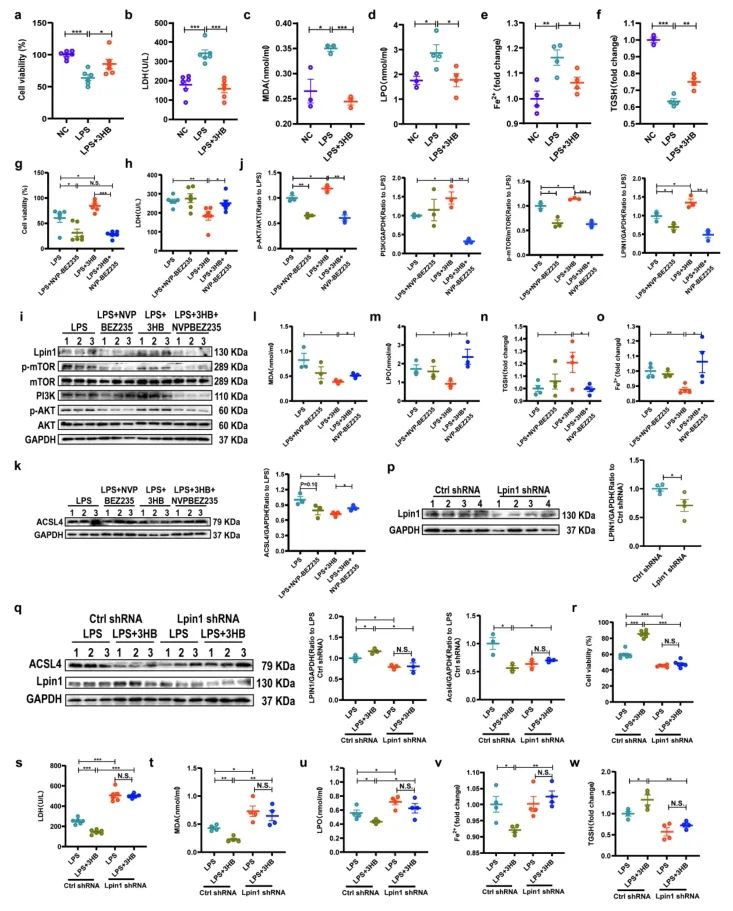
图6. 3-HB通过激活PI3K/AKT/mTOR/LPIN1通路抑制铁凋亡减轻AML12细胞损伤
研究结论
TRF通过调节肠道微生物群(特别是增加L. murinus的丰度)减轻脓毒症肝损伤,L. murinus通过促进3-HB的合成来发挥保护作用,3-HB激活PI3K/AKT/mTOR/LPIN1信号通路抑制肝细胞铁死亡,从而减轻脓毒症肝损伤。此外,血清3-HB水平与脓毒症患者的肝损伤指标呈负相关,可作为脓毒症肝损伤的潜在预测生物标志物,为临床管理和诊断脓毒症肝损伤提供了新知。
参考文献
Time-restricted feeding protects against septic liver injury by reshaping gut microbiota and metabolite 3-hydroxybutyrate. Gut Microbes. 2025
绘谱帮你测
该研究通过Q200宏代谢组学技术分析显示L. murinus处理显著提升脓毒症小鼠盲肠和血清中的3-羟基丁''酸(3-HB)水平,且3-HB与肝损伤标志物呈负相关,可作为脓毒症肝损伤的潜在预测生物标志物。
麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱已为数百家三甲医院、科研院所和企业提供多组学一站式整体解决方案,协助客户与合作伙伴发表SCI文章500+篇,累计影响因子5000+,平均IF>10,涵盖Cell, Science, Nature, Cancer Cell, Signal Trans-duction and Targeted Therapy, Nature Biotechnology, Cell Metabolism等权威期刊。
