
发表日期:2021年6月21
影响因子:14.919
研究方法:m6A meRIP-seq、RNA-seq
文章链接:METTL3 promotes tumour development by decreasing APC expression mediatedby APC mRNA N6-methyladenosine-dependent YTHDF binding
研究内容:
(1)METTL3上调与ESCC患者的低生存率相关
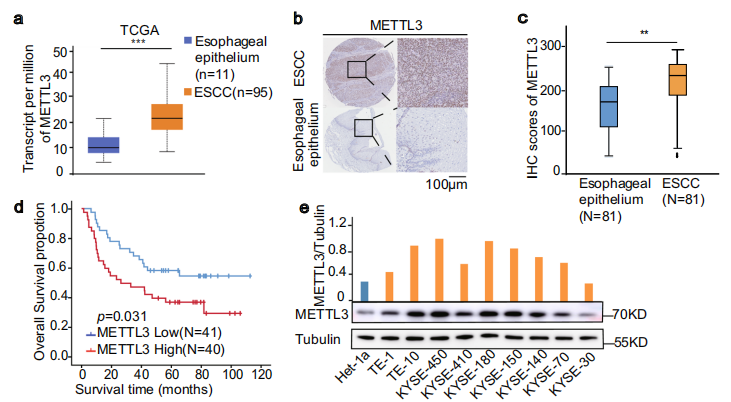
为了探讨METTL3在食管鳞癌中的表达情况,作者分析了TCGA数据发现与邻近正常食管上皮组织相比,食管鳞癌标本中METTL3的表达明显上调(Fig. 1a)。与此结果一致的是,对ESCC标本和邻近正常食管上皮组织进行免疫组化(IHC)染色(Fig. 1b,c)显示METTL3在ESCC组织中的表达水平显著高于相邻的正常组织。Kaplan-Meier分析显示,METTL3高表达的患者总生存时间短于低表达的患者(Fig. 1d)。同时METTL3 基因和蛋白(Fig. 1e)在9种不同的食管鳞癌细胞系中表达水平均高于正常食管上皮细胞。这些结果表明,METTL3在食管鳞癌中表达上调,且与食管鳞癌患者生存时间呈负相关。
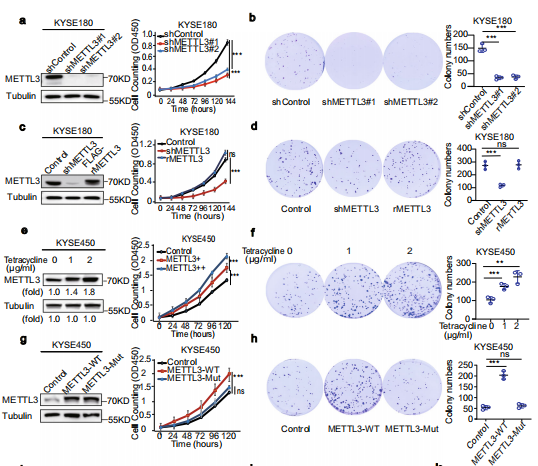
为了确定METTL3在细胞增殖中的作用,作者对METTL3进行了敲降。结果表明,METTL3的敲降减少了细胞的增殖(Fig. 2a)和集落数量(Fig. 2b)。这些抑制作用通过在KYSE180中重组表达一个耐RNA干扰的Flag-tagged mettl3恢复(Fig. 2c,d)。然后用四环素诱导表达在KYSE450细胞中的METTL3。四环素处理增加METTL3的表达且呈剂量依赖性,相应增加了细胞增殖水平(Fig. 2e)和集落形成(Fig. 2f)。与野生型(WT)相比,在ESCC细胞中过表达METTL3不活跃的突变体不能显著促进细胞的生长和增殖(Fig. 2g,h)。这些结果表明,METTL3促进肿瘤细胞增殖依赖于其表达水平和完整的活性。
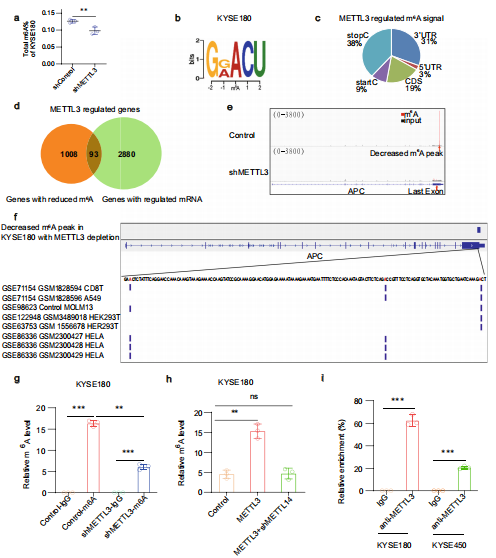
为了确定METTL3促进肿瘤细胞增殖的机制,作者检测了METTL3在ESCC细胞调控中的作用。METTL3 KO降低了KYSE180细胞中总m6A丰度(Fig. 3a)。m6A meRIP-seq和RNA-seq发现KYSE180中motif序列与m6A共识序列RRACH一致(Fig. 3b)。m6A信号在终止密码子和3’UTR区富集(Fig. 3c)。METTL3 KO中1101个基因中1199 m6A峰发生差异变化,RNA-seq显示有2973个基因发生了差异表达。在这些基因中,包括APC在内的93个基因存在重叠(Fig. 3d)。在METTL3 KO中m6A-MeRIP-seq中GO分析CC部分显示,β-catenin敲除复合物的基因组中m6A水平显著降低,包括APC。APC是Wnt负调控因子,促进β-连环蛋白降解。m6A峰位于APC终止密码子区附近的最后一个外显子,METTL3的耗尽降低了APC 的m6A水平(Fig. 3e)。miCLIP数据分析显示,APC 上有三个腺苷碱基被甲基化,并且位于METTL3 KO 后APC m6A峰的降低范围内(Fig. 3f)。这些结果表明,METTL3调控APC 的m6A水平。meRIP-qPCR检测METTL3 KO后APC 中m6A水平明显降低(Fig. 3g)。相反,METTL3过表达增加了APC中的m6A水平(Fig. 3h),这一现象受METTL14敲除恢复。此外,用METTL3抗体的RIP显示,METTL3在KYSE180和KYSE450细胞中与APC结合(Fig. 3i)。这些结果表明,METTL3与APC结合,并以METTL14依赖的方式提高其m6A水平。
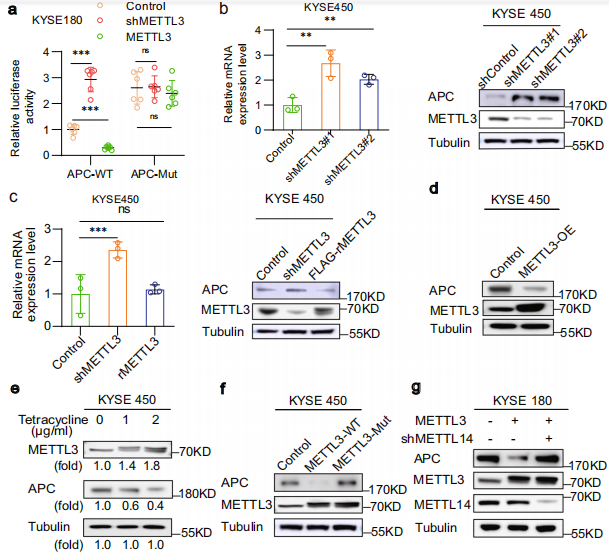
为研究METTL3依赖的m6A调控APC的表达,作者构建了一个荧光素酶报告基因,该基因具有完整的编码序列(CDS)包含WT或从3 '端突变的m6A APC 。荧光素酶分析显示,METTL3 KO极大地提高了WT APC的荧光素酶活性,而突变的APC提高了荧光素酶活性,并使该活性抵抗敲除METTL3的调控(Fig. 4a)。相反,METTL3过表达抑制WT APC的荧光素酶活性,但没有抑制突变体中APC的荧光素酶活性(图4)。这些结果表明,METTL3介导的m6A水平的上调抑制了APC的表达。
与这一发现一致的是,METTL3 KO增加了APC基因和蛋白的表达(Fig. 4b),而在KYSE450和KYSE180中重组表达METTL3则下调了这一增加(Fig. 4c)。此外,METTL3过表达降低了KYSE450细胞中APC的表达(Fig. 4d),而四环素剂量依赖性增加的METTL3表达水平与APC水平呈负相关(Fig. 4e)。相比之下,METTL3不活跃的突变体与其WT对应体不同,未能调节APC的表达(Fig. 4f)。值得注意的是,ESCC细胞中METTL3的消耗消除了METTL3过表达-降低的APC表达(Fig. 4g)。这些结果表明,METTL3介导的APC m6A上调协同抑制APC 基因和蛋白的表达ESCC细胞中的METTL14。
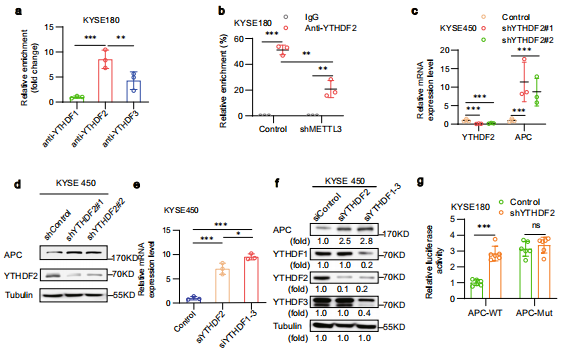
m6A Reader与m6A修饰的mRNA结合,导致蛋白表达增加或减少。YTHDF1-3介导mRNA降解。RIP-qPCR检测,发现YTHDF2结合APC 的数量远远高于KYSE180中YTHDF1和YTHDF3的数量(Fig. 5a)而METTL3敲除后(Fig. 5b)被还原。这些结果表明,METTL3增加APC 的m6A极大地促进了YTHDF2与APC 的结合。
为了研究YTHDF2与APC结合在APC表达中的作用,作者敲除了YTHDF2而后APC (Fig. 5c)和蛋白(Fig. 5d)在细胞中的表达增加。YTHDF1-3的联合敲除进一步增加了APC 基因(Fig. 5e)和蛋白(Fig. 5f)在这些细胞中的表达。此外,荧光素酶报告实验发现YTHDF2的缺失增强了含有m6A的WT APC CDS序列驱动的荧光素酶活性。然而突变的APC增强了荧光素酶的活性,并使该活性抵抗YTHDF2 敲除的调控(Fig. 5g)。这些结果表明mett3增加APC 的m6A,随后结合YTHDF抑制APC的表达。
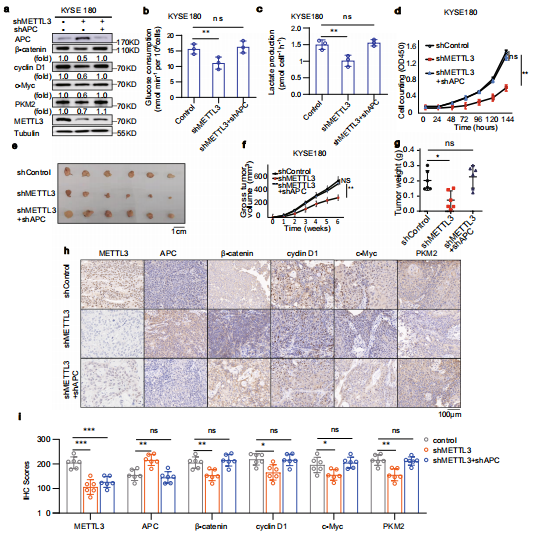
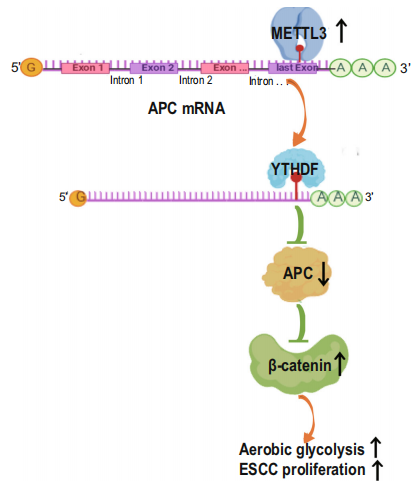
APC功能的缺失可以稳定β-catenin,诱导下游基因的表达(如CCND1和MYC)。促进细胞周期进程,而cMyc(由MYC编码)通过上调糖酵解基因的表达来促进有氧糖酵解。METTL3缺失增强了KYSE180中APC的表达,降低了β- catenin、cyclin D1、c-Myc和PKM2的表达(Fig. 6a)。然而,METTL3过表达降低了KYSE180中APC的表达,增强了β-catenin、cyclin D1、c-Myc和PKM2的表达。此外,METTL3 KO降低了葡萄糖摄取(Fig. 6b)、乳酸产量(Fig. 6c)、细胞增殖(Fig. 6d)和细胞集落数量。值得注意的是,这种METTL3 KO引起的基因表达的抑制(Fig. 6a),糖酵解(Fig. 6b,c),细胞增殖和菌落形成在APC KO后大部分消失。这些结果表明,METTL3降低APC的表达,促进β-catenin介导的下游基因表达,有氧糖酵解和ESCC细胞增殖。
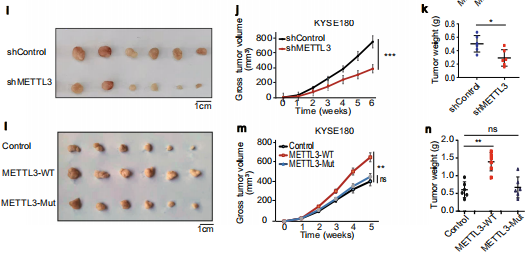
为了确定METTL3诱导的APC表达下调在小鼠肿瘤生长中的作用,作者进行了皮下注射实验。结果发现,METTL3的KO减少了肿瘤的大小(Fig. 6e)、体积(Fig. 6f)和重量(Fig. 6g),以及肿瘤组织中的乳酸含量,这一过程可通过APC KO恢复。此外,IHC染色显示,METTL3 KO增加了肿瘤组织中APC的表达,相应的β-catenin、cyclin D1、c-Myc和PKM2的表达降低(Fig. 6h,i)。这些结果表明,通过METTL3抑制APC表达促进肿瘤的发展。
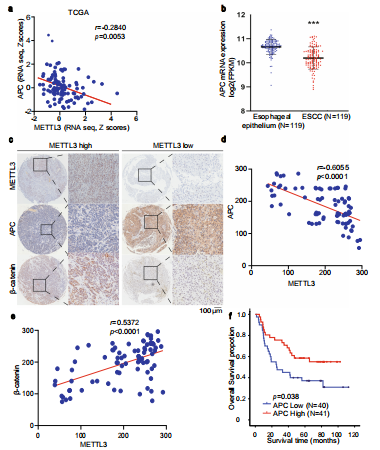
为了确定METTL3抑制APC表达的临床相关性,作者进行了TCGA数据分析,显示APC 的表达为与食管鳞癌中METTL3 的表达呈负相关(Fig. 7a)。此外,对119对ESCC标本及其邻近正常组织进行基因表达谱分析,发现APC表达明显在ESCC中显著下调(Fig. 7b),免疫组化染色发现METTL3蛋白表达与APC蛋白表达成负相关(Fig. 7c,d),而与β-catenin蛋白表达呈正相关(Fig. 7c,e)。此外,APC的高表达与ESCC患者较长的总生存时间显著相关(Fig.7f)。上述结果说明APC表达下调与人类METTL3表达上调相关且导致食管鳞癌患者预后差。
1.m6A RNA修饰测序
MeRIP-seq
通过使用m6A抗体富集高甲基化的RNA的片段,然后结合高通量测序,在全转录组范围内研究发生m6A的区域
2.m6A RNA修饰靶基因验证
MeRIP-qPCR
云序提供m6A的MeRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证m6A修饰靶基因表达水平。
3.机制互作研究
RIP-seq/qPCR
筛选或验证m6A修饰直接靶点,研究m6A修饰靶基因的调控机制。
RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
4.RNA修饰上游酶的筛选
RNA修饰相关酶PCR芯片
寻找上游直接调控m6A甲基化的甲基转移酶。
5.检测整体m6A RNA修饰水平
LC-MS/MS检测整体RNA修饰水平
精zhun高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体m6A甲基化水平
周期短、RNA起始量小,低至200ng。
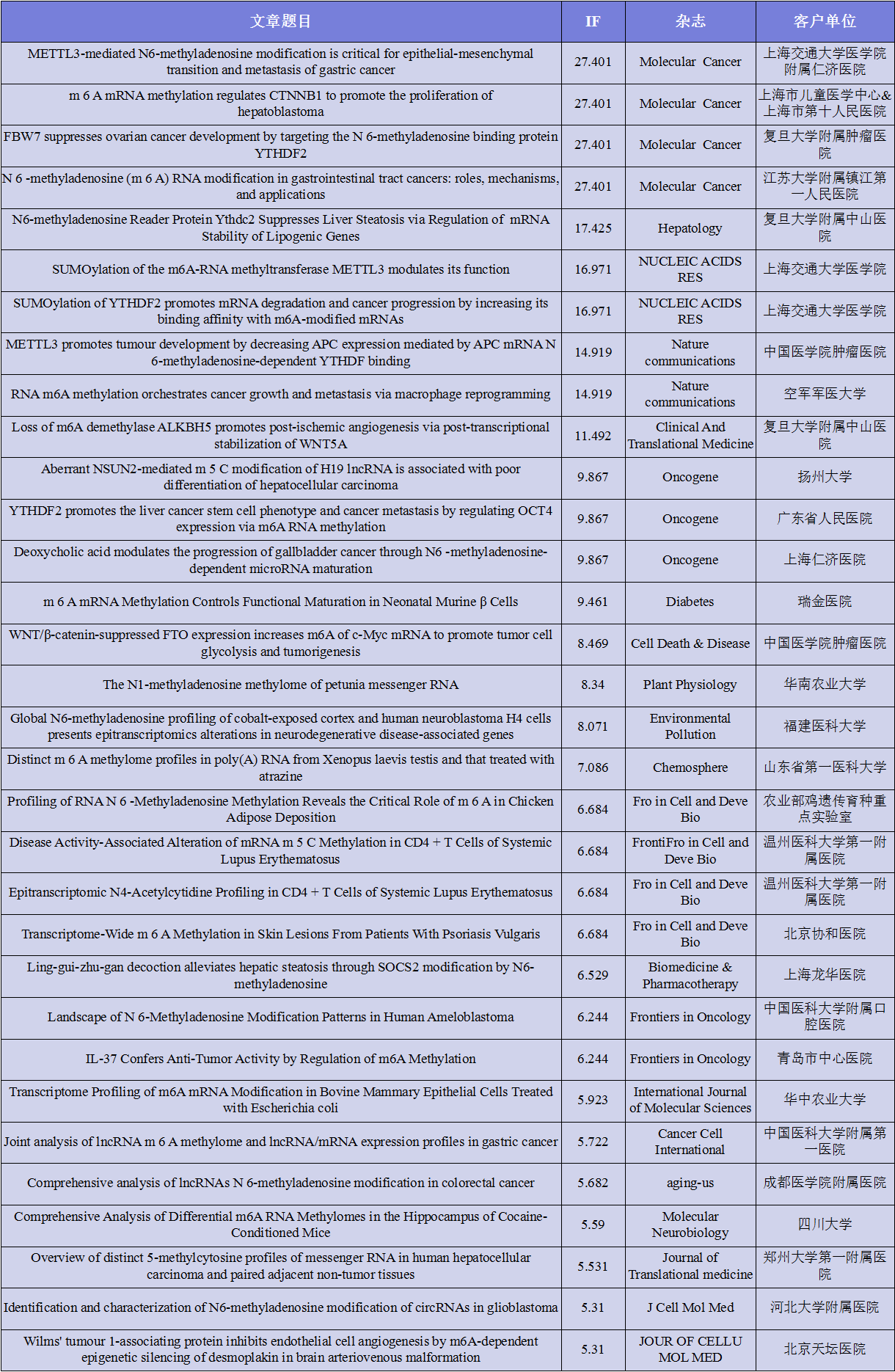
云序客户RNA修饰文章列表
相关产品
m6A RNA甲基化测序
m5C RNA甲基化测序
m1A RNA甲基化测序
RNA乙酰化测序
m7G (m3C)RNA 甲基化测序
2’-O-RNA甲基化测序
RIP测序
全转录组测序
比色法检测整体m6A甲基化水平
LC-MS/MS检测核酸修饰水平
RNA修饰相关酶PCR芯片
ChIP测序
CoIP
往期回顾
经典思路|云序客户circRNA+m6A案例教您快速发表5分文章
农口方向3个月内搞定5分文章秘籍——m6A热点错不了
